

本文共计10,210字,建议阅读时间18分钟
商业成功是专利创造性判断的辅助因素之一。《专利审查指南》明确规定,发明是否具备创造性,通常应当根据本章第3.2节所述的审查基准(即“三步法”)进行审查。应当强调的是,当申请属于以下情形时,审查员应当予以考虑,不应轻易作出发明不具备创造性的结论……其中,“发明在商业上获得成功”即为情形之一。
以上对“商业成功”作为专利创造性判断辅助因素的定位也在司法实践中予以遵循。国家知识产权局与胡颖、深圳市恩普电子技术有限公司实用新型专利权无效行政纠纷案[1](下称“超声检测仪案”)中,最高人民法院(下称“最高院”)指出,对技术方案创造性的评价,一般会从对现有技术作出贡献的角度出发,采取相对客观的“三步法”判断方式,判断要求保护的技术方案是否对现有技术构成了实质上的“贡献”,从而决定是否对其授予专利权。当采取“三步法”难以判断技术方案的创造性或者得出技术方案无创造性的评价时,从社会经济的激励作用角度出发,商业上的成功就会被纳入创造性判断的考量因素。
既然“应当”予以考虑,实践中,又在多少案件中被实际考虑?未被考虑的原因是什么?企业应如何基于商业成功主张创造性?本文尝试以医药领域案件为例,对这些问题予以解答。
一、涉及商业成功的医药领域案件
经初步检索及人工筛选,共获得22件涉及商业成功的医药领域行政诉讼案件及29件无效案件(见下表)。
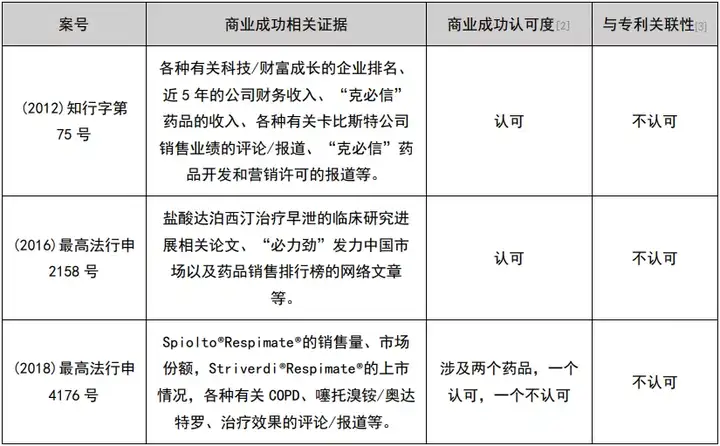
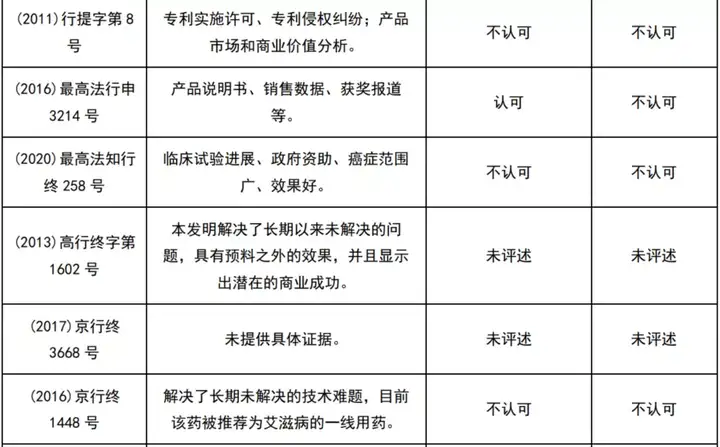
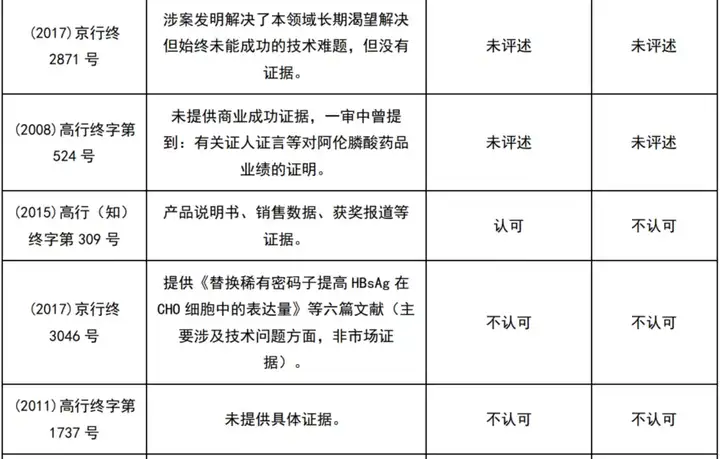
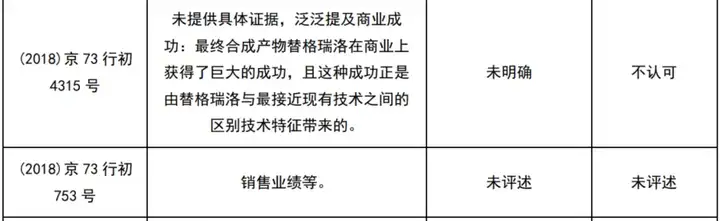
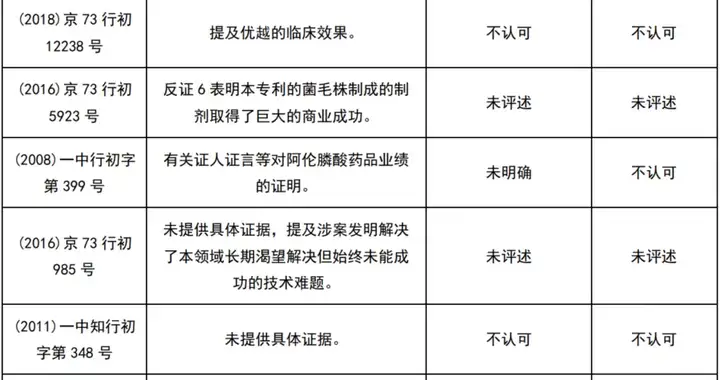
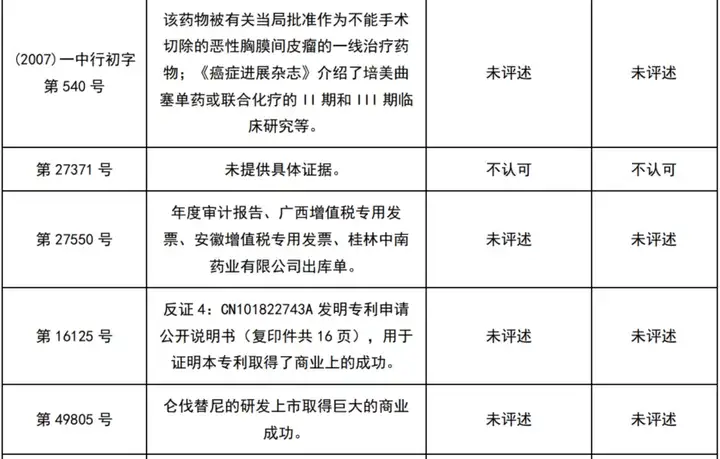
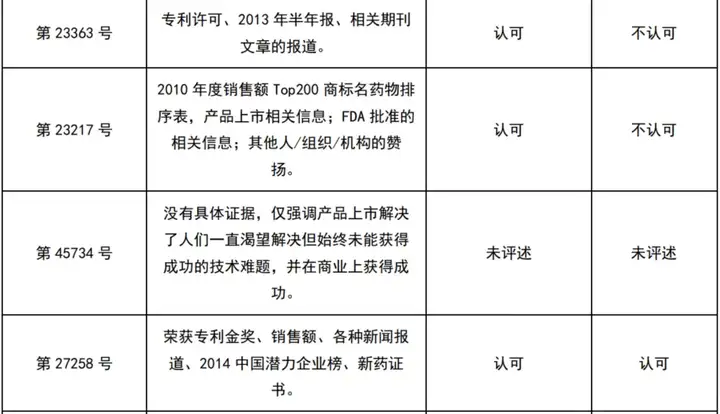
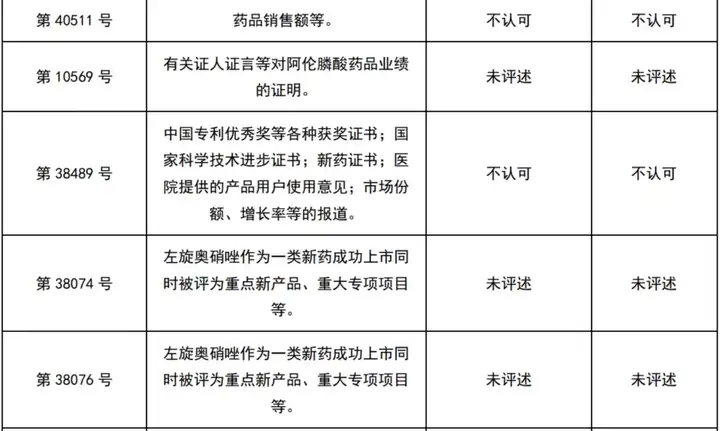
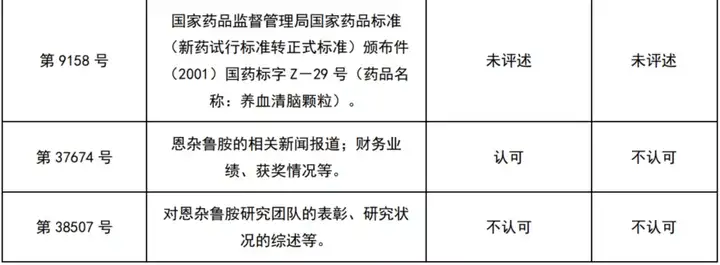
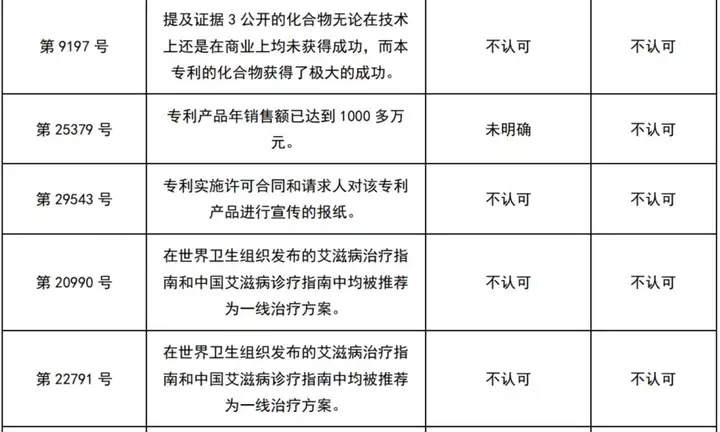
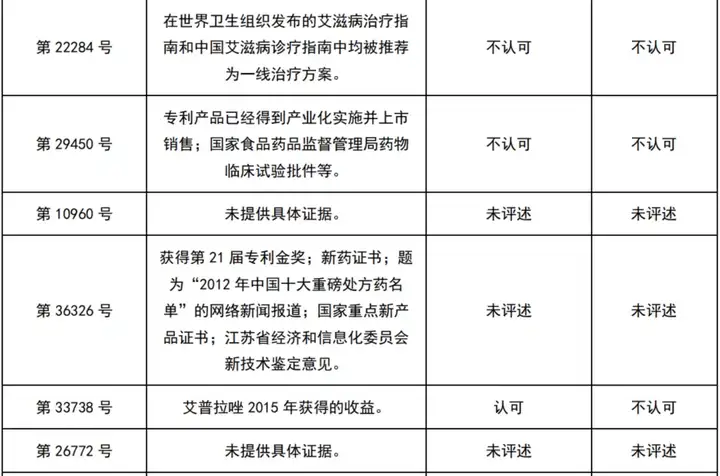

这51个案件中,认可商业成功的9件(区别于专利法意义上的商业成功,仅指确实有商业上的成功存在,而不论其原因),而最终得到支持的仅1件。
该唯一得到支持的案件(第27258号无效决定)涉及发明名称为“新型作为酪氨酸激酶抑制剂的稠合的喹唑啉衍生物”、申请号为03108814.7的专利,专利权人为贝达药业股份有限公司。请求人针对案涉专利提出无效宣告请求,专利权人提供荣获专利金奖、销售额、各种新闻报道、2014中国潜力企业榜、新药证书等证据证明专利化合物商业上获得成功,进而论证专利化合物具备创造性。合议组认为就专利权利要求9所保护的化合物、特别是权利要求9的最后一个化合物(即埃克替尼)而言,该药品于2011年6月获得新药证书、8月上市,当年销售额即为6000万人民币,两年后年销售额则近5亿人民币,可见,该药品确实在短时间内在商业上获得成功,故埃克替尼于短时间内在商业上获得成功也佐证了本发明化合物具有创造性,佐证了本发明的发明构思相对于现有技术是有贡献的。该案件还提到,“由于药物化学领域是严重依赖技术支持、技术革新的领域,只有研发出确实安全有效的药物时,所述药物才能被批准上市才能被广大病患所接受,进而产生相应的商业效益。”可见,医药领域主张“商业成功”对创造性的支撑是可行的[4]。
既然可行,以“商业成功”佐证专利创造性,为什么总是不成功呢?
二、“商业成功”为什么难以成功?
《专利审查指南》及司法判例对如何判断商业成功给出了指引。
《专利审查指南》规定,“当发明的产品在商业上获得成功时,如果这种成功是由于发明的技术特征直接导致的,则一方面反映了发明具有有益效果,同时也说明了发明是非显而易见的,因而这类发明具有突出的实质性特点和显著的进步,具备创造性。但是,如果商业上的成功是由于其他原因所致,例如由于销售技术的改进或者广告宣传造成的,则不能作为判断创造性的依据。”
在贝林格尔英格海姆法玛两合公司与国家知识产权局驳回复审行政纠纷案(下称“奥达特罗案”)[5]中,最高院指出,相比相对客观的“三步法”而言,对商业成功的审查应当秉持相对严格的标准。当申请人主张其发明获得了商业上的成功时,应当审查:其一,相关证据能否证明与发明对应的技术方案取得了商业上的成功;其二,该商业上的成功是否源于发明的技术方案相对现有技术作出改进的技术特征,而非其他因素所导致。相应地,必须对发明取得商业成功的原因进行分析,排除销售策略或广告宣传等技术特征之外的其他因素对发明取得商业成功的影响,只有在发明的技术方案与现有技术的区别技术特征之间存在直接的因果关系的情形下,才能反推发明的技术方案是非显而易见的,从而认定发明具有创造性。
总结《专利审查指南》相关规定以及最高院的观点,并基于对案件的梳理和分析,笔者认为,证明“商业成功”需要满足以下四个条件:1.存在商业上的成功(下称“条件1”);2.商业上的成功与发明的技术方案有对应性(下称“条件2”);3.商业上的成功源于发明的技术方案相对现有技术作出改进的技术特征(下称“条件3”);4.合理排除其他原因如销售技术或者广告宣传的影响(下称“条件4”)。
以下将结合4个医药领域案件进行具体说明。
案例一 达托霉素案
达托霉素( Daptomycin )是卡比斯特(Cubist)公司开发的环脂肽类抗生素。2003年底,美国FDA经过快速审理程序批准注射用达托霉素(商品名cubicin,克必信)用于治疗由革兰氏阳性敏感菌株引起的并发性皮肤及皮肤结构感染。2014年默沙东以95亿美元收购卡比斯特公司,获得克必信产品。根据公开资料,克必信2016年全球销售额超过10亿美元。
达托霉素最早是由礼来公司研发,但礼来公司在临床研究中发现当使用达托霉素治疗深度细菌感染的患者时,高频率给药治疗一段时间后,部分患者会出现短暂的肌肉无力和疼痛等不良反应,并产生附带的骨骼肌毒性,无法开展临床应用。卡比斯特公司接手后继续开发,通过低频率高浓度方式给药能够将患者的骨骼肌毒性降低到最低限度。基于该研发成果,卡比斯特公司于1999年9月24日向国家知识产权局申请了名称为“抗生素的给药方法”的发明专利,并于2004年5月19日获得授权,专利号为99812498.2。
请求人于2008年6月4日向专利复审委员会提出专利权无效宣告请求。专利复审委员会于2009年04月07日作出宣告第99812498.2号发明专利权全部无效的决定[6]。无效决定作出后,卡比斯特公司向北京市第一中级人民法院提起行政诉讼[7],一审败诉后又向北京市高级人民法院提起上诉,但二审驳回上诉,维持原判[8]。2012年,卡比斯特公司向最高院申请再审[9]。
最高院认可卡比斯特公司提交的近5年公司财务收入、“克必信”药品收入、各种有关卡比斯特公司销售业绩的评论/报道等证据,认为其能够证明“克必信”药品已取得商业成功,即满足条件1。
克必信是用于治疗细菌感染的药物,其有效成分为潜霉素(即达托霉素),而案涉专利保护的是潜霉素在制备用于治疗有此需要的患者细菌感染的药剂中的用途,商业上的成功与发明的技术方案有对应性,即满足条件2。
对于条件3,应当先找出“发明的技术方案相对现有技术作出改进的技术特征”,然后再去判断商业上的成功是否源于改进。就达托霉素案而言,案涉专利权利要求1主张“潜霉素在制备用于治疗有此需要的患者细菌感染而不产生骨骼肌毒性的药剂中的用途,其中用于所述治疗的剂量是3-25mg/kg的潜霉素,其中重复给予所述的剂量,其中所述的剂量间隔是每隔24小时一次至每48小时一次(无效宣告过程中,专利权人修改后的权利要求)。”现有技术-证据6公开了在2mg/kg每24小时剂量下,潜霉素显示出有效治疗多种革兰氏阳性感染,在3mg/kg每12小时的剂量下注意到偶发的副作用,并公开了潜霉素的抗菌机理。因此,权利要求1与证据6的区别在于“不产生骨骼肌毒性”和“其中所述治疗的剂量是3-25mg/kg的潜霉素,其中重复给予所述的剂量,其中所述的剂量间隔是每隔24小时一次至每48小时一次”。
然而,根据《专利审查指南》的有关规定,给药对象、给药方式、途径、用量及时间间隔等仅仅体现用药过程的特征不构成对权利要求的限定。因此,该案中,最高院最终认定“不产生骨骼肌毒性”和“其中所述治疗的剂量…每48小时一次”没有限定作用,因而也就不可能认定这些特征做出了贡献,即未满足条件3。
结合笔者前面对达托霉素发展历史的介绍,可以发现卡比斯特公司“通过低频率高浓度方式给药能够将患者的骨骼肌毒性降低到最低限度”是有贡献的,如果《专利审查指南》未限制给药对象、给药形式、给药剂量、时间间隔等对权利要求的限定作用,本案或许有不同的结果。
案例二 达泊西汀案
达泊西汀是一种短效选择性5-羟色胺再摄取抑制剂(SSRIs),化学名为S-(+)-N,N-二甲基-a-[2-(萘氧基)乙基]苯甲胺。药物原理是通过抑制5-羟色胺再吸收,增加突触间隙5-HT活性,从而延迟射精冲动,治疗早泄,被誉为“延时伟哥”,适用于治疗18至64岁男性早泄(PE)患者。
达泊西汀最早由礼来公司开发,2003年被出售给强生,并于2004年以治疗早发性射精的适应症向FDA申报审批,但达泊西汀仍未获得FDA批准。在美国之外,达泊西汀已在全球32个国家和地区正式上市,在中国的商品名为“必利劲”,也是唯一获得批准治疗PE适应证的药物。
APBI公司是专利号为00815313.2、名称为“利用快速起效的选择性5-羟色胺再摄取抑制剂来治疗性功能障碍的方法”发明专利的专利权人。授权公告的权利要求书1为:达泊西汀或其可药用盐在生产用于治疗或控制哺乳动物性功能障碍的药物中的应用。
请求人于2012年5月23日向专利复审委员会提出专利权无效宣告请求。无效过程中,APBI公司将权利要求1修改为“达泊西汀或其可药用盐在生产用于治疗或控制哺乳动物性功能障碍的药物中的应用,其中所述药物是口服固体剂型。”专利复审委员会于2012年12月27日作出宣告专利权全部无效的决定。无效决定作出后,APBI公司向北京市第一中级人民法院提起行政诉讼[10],一审败诉后又向北京市高级人民法院提起上诉,但二审驳回上诉,维持原判[11]。2016年,APBI公司向最高院申请再审[12]。
APBI公司再审申请中提交第三组证据(即证据7-10)用于证明案涉专利取得了商业上的成功。证据主要涉及盐酸达泊西汀治疗早泄的临床研究进展相关论文、“必力劲”发力中国市场以及药品销售排行榜的网络文章等。最高院认可“必力劲”药品取得商业成功,即满足条件1。
案涉专利保护达泊西汀或其可药用盐在生产用于治疗或控制哺乳动物性功能障碍的药物中的应用,而“必利劲”是批准治疗PE适应证的药物,有效成分为达泊西汀,商业上的成功与发明的技术方案有对应性,即满足条件2。
对比文件1公开了包括达泊西汀或其盐、达泊西汀分离的异构体或其盐在内的物质或组合物在治疗疾病的方法中的用途。其所公开的达泊西汀治疗早泄、性功能障碍的技术方案中,还公开了早泄的定义以及治疗可获得的效果(虽然对比文件1中并列技术方案数量庞大,但不影响其公开了所述技术方案)。权利要求1与对比文件1的区别在于剂型的选择等。
仅就区别特征“口服固体剂型”而言,通过“三步法”很难认定具有创造性贡献。如果申请人主张商业成功作为辅助因素以佐证创造性,则需证明商业成功源于“口服固体剂型”,在提交证据时至少需要提交口服固体剂型与非口服固体剂型的销售数据对比等。同时还需要注意条件4的满足,即注意合理排除其他原因如销售技术或者广告宣传的影响。本案中,申请人并未提交比对数据,也未合理排除其他原因,最高院最终认定“不能证明该商业成功是由于本发明中对权利要求有具体限定作用的、使其区别于现有技术的技术特征直接导致的。”
案例三 来那度胺案
来那度胺是由美国赛尔金(Celgene)公司开发的抗肿瘤药物,化学名为3-(7-氨基-3-氧代-1H-异吲哚-2-基)哌啶-2,6-二酮,具有抗肿瘤、免疫调节和抗血管生成等多重作用。来那度胺最早于2005年被FDA批准用于治疗骨髓增生异常综合征,随后2007年被FDA批准用于多发性骨髓瘤,到2013年,又被FDA批准用于套细胞淋巴瘤。随着适应症的不断拓宽,销售额也一路飙升,2016年销售额为69.74亿美金,2017年销售额是81.87亿美金,2018年销售额达到96.85亿美金。
来那度胺的化学结构与沙利度胺相似。沙利度胺在20世纪50至60年代初期在全世界广泛使用,它能够有效地阻止女性怀孕早期的呕吐,但也妨碍了孕妇对胎儿的血液供应,导致大量“海豹畸形婴儿”出生(即“反应停”事件),因此沙利度胺被禁用了40多年。后研发人员不断对沙利度胺进行结构改进,通过将沙利度胺左边的邻苯二甲酰亚胺用异吲哚啉酮取代,并在4-位引入氨基得到了来那度胺。
基于上述研发成果,赛尔金公司于1997年7月24日向国家知识产权局申请了名称为“取代的2-(2,6-二氧哌啶-3-基)-邻苯二甲酰亚胺和-1-氧异二氢吲哚及降低肿瘤坏死因子α的方法”的发明专利,并于2003年8月6日获得授权,专利号为97180299.8。授权公告的权利要求1保护下式所示的化合物。
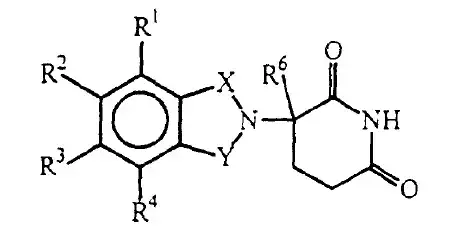
从公开资料来看,该专利先后被杜兆东、北京淦航医药科技有限公司、南京卡文迪许生物工程技术有限公司提出专利权无效宣告请求。
针对南京卡文迪许生物工程技术有限公司的无效宣告请求,专利复审委员会作出宣告专利权全部无效的决定。无效决定作出后,赛尔金公司向北京市第一中级人民法院提起行政诉讼,一审败诉后又向北京市高级人民法院提起上诉,但二审驳回上诉,维持原判[13]。2016年,赛尔金公司向最高院申请再审[14]。
赛尔金公司再审申请中提交产品说明书、销售数据、获奖报道等证据用于证明案涉专利取得了商业上的成功(裁判文书中未详细公布具体的证据)。来那度胺市场空间巨大,属于“重磅炸弹”级药物,商业上无疑是成功的,即满足条件1。
案涉专利为来那度胺的化合物专利,商业上的成功与发明的技术方案有对应性,即满足条件2。
现有技术-证据6公开了具体化合物沙利度胺和沙利度胺的衍生物EM-12。证据6还公开沙利度胺或沙利度胺衍生物可以控制TNF-α的异常浓度。案涉专利权利要求1相对于证据6公开的化合物EM-12的区别特征仅在于权利要求1指向的具体化合物在异二氢吲哚环的4位上具有氨基取代基。
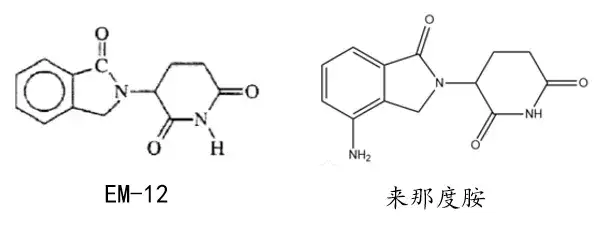
最高院认为在证据6已经公开EM-12的基础上,为获得结构类似、活性相当的替代化合物,有动机根据证据6通式化合物部分公开的内容在4位上引入氨基取代基,这属于常规的结构修饰。如前所述,当采取“三步法”否定了技术方案的创造性时,商业上的成功应当被纳入创造性判断的考量因素。由于裁判文书中未详细公布具体的证据,我们无法判断赛尔金公司是否提供证据以证明案涉专利权利要求1相对于证据6的区别技术特征与商业成功之间具有关联性,从裁判结果来看,答案应该是否定的。值得思考的是,EM-12很可能是未商业化的药物,再考虑到沙利度胺的“不成功”,来那度胺的商业成功难道不是因区别技术特征带来的吗?
案例四 奥达特罗案
奥达特罗是由贝林格尔英格海姆法玛两合公司(下称“贝林格尔公司”)研发的用于治疗慢性阻塞性肺疾病(COPD)及哮喘的新分子实体。化学名为6-羟基-8-[(1R)-1-羟基-2-[[2-(4-甲氧基苯基)-1,1-二甲基乙基]氨基]乙基]-2H-1,4-苯并噁嗪-3(4H)-酮。2014年7月31日在美国上市,商品名Striverdi Respimat。
奥达特罗作为β2受体激动剂能够提高气道平滑肌细胞内cAMP水平,通过松弛气道平滑肌实现气管舒张的作用,已成为目前主要的慢性阻塞性肺疾病治疗药物。贝林格尔公司还将奥达特罗与噻托溴铵联合使用,商品名为Stiolto Respimat(在中国称为思合华®能倍乐®),两种药物可实现机制互补,协同增效,进一步改善慢阻肺的气流受限,从而帮助患者更顺畅的呼吸。
目前,全球范围内哮喘患者约有3.34亿人,COPD患者约有3.28亿人。COPD是中国第三大慢性疾病,有近1亿患者。呼吸系统疾病的药物全球市场超过200亿美元,而Striverdi Respimat、Stiolto Respimat为其中的畅销药。
贝林格尔公司于2003年11月11日向国家知识产权局申请了名称为“用于治疗慢性阻塞性肺病的新药物”的发明专利,申请号为200380103094.5,2009年提出分案申请200910266327.2。2012年06月01日国家知识产权局驳回了该分案申请,贝林格尔公司提起复审,2014年12月10日专利复审委员会作出维持决定。后贝林格尔公司向北京市第一中级人民法院提起行政诉讼,后又向北京市高级人民法院提起上诉,二审驳回上诉,维持原判[15]。2018年,贝林格尔公司向最高院申请再审[16]。
贝林格尔公司再审申请中提交两组证据用于证明案涉专利取得了商业上的成功。证据主要涉及Spiolto®Respimate®的销售量、市场份额,Striverdi®Respimate®的上市情况,各种有关COPD、噻托溴铵/奥达特罗、治疗效果的评论/报道等。最高院认可Spiolto®Respimate®药品取得商业成功,即满足条件1。
案涉专利申请权利要求1请求保护的式1a化合物奥达特罗,仅是Spiolto中两种活性成分之一。最高院认为贝林格尔公司证明Spiolto获得商业成功的证据都是针对两种活性成分联合用药之后取得的效果,现有证据不能证明贝林格尔公司所主张的Spiolto的商业成功是奥达特罗直接导致的。即,商业上的成功与发明的技术方案不对应,不满足条件2。
本案中值得注意的是贝林格尔公司还有一款上市药品Striverdi,其唯一活性成分为奥达特罗,与发明的技术方案完全对应,然而贝林格尔公司并未提供Striverdi有关的充足证据来证明商业上取得成功。
通过以上分析,可以看出,国家知识产权局及法院对商业成功的认定均秉持严格的标准,这对专利申请人或权利人的举证提出了很高的要求。那么,如何举证呢?
三、举证建议
笔者认为,可以从证明“商业成功”需要满足的四个条件入手。
1.证明存在商业上的成功
较为直接的证据有药品销售量、销售金额、市场份额、审计报告、财报等;辅助证据有新闻/期刊/论文等的评论/报道;专利许可/实施情况;获奖情况;政府资助情况;临床进展/批件;其他人/组织/机构的赞扬/推荐等。
值得注意的是,最高院在前述超声检测仪案中提到“成功与否应当由该发明或者实用新型所代表的技术或产品相比其他类似的技术或产品在同行业所占的市场份额来决定,单纯的产品销售并不能代表已经取得商业上的成功”,这说明除非提供的销售量/销售金额数值非常大,使得裁判者对商业上获得成功没有疑虑,否则最好同时提供参比数据。
2.证明商业上的成功与发明的技术方案有对应性
一个药品会涉及化合物专利(通式化合物、药学上可接受的盐、活性代谢产物、前药、手性药物光学异构体、中间体等)、晶型专利(单晶、多晶、共晶、无定型等)、组合物专利、用途专利(用途、新适应症等)、制剂专利、检测/分析专利、制药设备等,提交证据时需要整体考虑案涉专利具体保护什么样的技术方案,根据技术方案来筛选证据。比如新适应症专利,笼统的销售数据恐难以证明与新适应症的一一对应关系。又比如前述奥达特罗案,上市药品Striverdi与专利的对应性明显好于Spiolto,准备证据时自然应当侧重于Striverdi的销售量、销售金额、市场份额、专项审计报告等。
3.证明商业上的成功源于发明的技术方案相对现有技术作出改进的技术特征
这一证明要件具有相当的难度,比如前述来那度胺案,如何去证明“在异二氢吲哚环的4位上引入氨基取代基”这一改进技术特征对商业上的贡献?如果市场上存在活性成分为EM-12的药品,则较为容易,通过提交一系列来那度胺与EM-12药品的对比数据(包括销量、药品定价、药效、副作用、市场份额、增长率、对患者生活方式的改变、获批的范围、销售的地域范围等)能够较为清楚的证明。如果不存在活性成分为EM-12的药品,则一旦提交其他参比对象,很可能裁判者会认为即使证明相对于其他参比对象取得了成功,也仍然无法证明商业上的成功源于改进的技术特征。笔者认为对于不可能完成的证明内容,裁判者不应过于苛责。一般而言,市场上同靶点或相同适应症的药物远不止一个,通过横向比较结构类似的化合物,纵向比较同靶点、同适应症的药物,并尽可能的多角度展开比对,则有可能被接受。
另外,竞争对手、仿制药厂商在新药申请、市场宣传等方面可能会披露对药品市场价值的看法,尤其是无效宣告请求人的一些自认,可以作为补充证据。
4.合理排除其他原因如销售技术或者广告宣传的影响
在目前梳理出的51个案件中,基本没有案件详细论述销售技术或者广告宣传的影响。一个新药品上市,必然会进行一定的市场营销,笔者认为这本身并没有什么问题。所谓合理排除其影响,从证据的角度来说,可以比较医药市场通常的营销强度,同等水平的竞争对手推广的手段、费用,同靶点、同适应症药物的营销情况等,如果并未采取特殊的营销策略,也没有使用显著高的推广费用,但却取得了非常高的市场份额、快速的市场增长率等,则可以合理排除销售技术或者广告宣传的影响。
注释:
[1] (2012)行提字第8号
[2]此处商业成功区别于专利法意义上的商业成功,仅指确实有商业上的成功存在,而不论其原因、是否与专利技术对应。
[3]“关联性”指商业上的成功是否与案涉专利对应/相关联。
[4]有趣的是,在第38507号无效决定中,专利权人也提供了商业成功的证据,并且引用第27258号案件以支持自己的主张,合议组认为,“反证9(即第27258号案件)和审理的案件情形不同,反证9的化合物本身就具备创造性,在此基础上讨论了其商业成功是源于技术原因,从而可以佐证其具备创造性,而不是仅以商业成功作为判断创造性的标准。”
[5](2018)最高法行申4176号
[6]第13188号无效宣告请求审查决定。
[7](2009)一中行初字第1847号
[8](2010)高行终字第547号
[9] (2012)知行字第75号
[10](2013)一中知行初字第3245号
[11] (2014)高行终字第1706号
[12](2016)最高法行申2158号
[13](2015)高行(知)终字第309号
[14] (2016)最高法行申3214号
[15](2017)高行终第3668号
[16](2018)最高法行申4176号
免责声明
本文及其内容仅为交流目的,不代表天同律师事务所或其律师出具的法律意见、建议或决策依据。如您需要法律建议或其他专业分析,请与本文栏目主持人联系。本文任何文字、图片、音视频等内容,未经授权不得转载。如需转载或引用,请联系公众号后台取得授权,并于转载时明确注明来源、栏目及作者信息。


天同说知产!一同说知产!“同说知产”栏目聚焦知识产权理论与实务中的热点、难点问题,我们希望借此栏目搭建知识产权理论与法律实务、商业实践的衔接、交流互动平台。如您有任何想法、意见、建议,欢迎点击文末留言。
向“同说知产”栏目投稿,欢迎发送邮件至:
zhaoxu@tiantonglaw.com
suzhifu@tiantonglaw.com