


生物医药作为新兴技术与关键技术密集的重要领域,受关注度正不断提升。然而,国内药企欲从境外引进生物医药技术或通过对外授权打入国际市场,当前可能都将面临国际范围内进出口管制政策变化的影响,跨境License-in/out阻力增加,一些跨境技术交易进程已经被搁置或被取消,这更加深了药企的担忧。
2022年9月12日,美国白宫官网发布简讯宣布,总统拜登签署行政命令,启动“国家生物医药技术和生物制造倡议”。有评论认为,该行政命令是个“风向标”,未来美国对中国的技术限制可能从芯片、能源扩大到生物领域。[1] 2022年10月27日,《华盛顿邮报》报道,商务部负责工业和安全的副部长艾伦·埃斯特维兹(Alan Estevez)表示,生物医药技术将可能是实施额外出口管制的重点领域。[2] 2022年10月31日,《彭博社》报道,美国官员正在与欧盟同行讨论收紧对中国出口限制的可能性。[3]上述政策变化或释放出缩紧跨境技术交易的信号,对国内药企影响深远。本文针对跨境License-in/out可能面临的技术进出口限制进行简要梳理与分析,以期为药企提供一定的参考。

美、欧的生物医药技术出口强监管信号
美国一直将生物医药作为国家的关键技术领域。在出口、外资准入方面都采取了一系列强监管措施以防止技术外流,保持其在生物医药领域的国际领先地位。根据美国商务部工业与安全局(Bureau of Industry and Security,BIS)制定的《出口管理条例》(Export Administration Regulation,EAR),向外国公民或其他主体转让/披露受控技术(包括提供技术服务、披露技术数据等)构成“视同出口”行为。EAR着重针对“军民两用物品/技术的管制”,管制清单为《商业限制清单》(Commerce Control List,CCL)。CCL将限制物项分为十类和五组,与生物医药相关的主要是第1类“微生物和毒素(Microorganisms and Toxins)”。CCL下所有受管制的物项都使⽤出⼝管制分类编码[4](Export Control Classification Number,ECCN)进行编排。当前CCL清单下与生物医药相关的受控技术主要有:
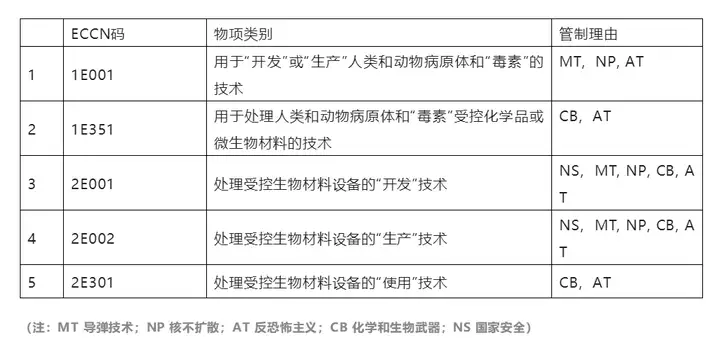
上表中,涉及病原体、毒素的技术被列入管制清单,主要原因在于其具有“双重用途”,既可用于合法制造药品也可用于生产生化武器,对其进行出口管制可有效控制生化武器扩散对国家安全造成的威胁。医药技术通常专注于研究和寻找疾病的诊断和治疗方法,拯救患者的生命,除涉及生物恐怖主义和毒素之外几乎不太会引起对国家安全的担忧,因此较少受到EAR的影响。
然而,近几年,以上情况可能发生变化。2018年美国国会通过了《出口管制改革法案》(the Export Control Reform Act,ECRA),该法案提出扩大对新兴和基础技术(包括生物医药技术)的出口管制。2018年11月,在针对该法案发布的拟议修法的提前通知(ANPRM)中,BIS进一步强调生物医药技术是一种新兴技术(也称为第1758条技术),对国家安全至关重要。ECRA是EAR的上位法,现行有效的EAR也根据该法案的内容进行了一定的修改。随着美国政府将生物医药技术等新兴技术确定为未来产业,并把以前对军事和军民两用技术的限制扩大到了“新兴和基础技术”领域,EAR中的《商业限制清单》已经不能满足目前的管制需求,很多“新兴技术”并不符合此前已有特定ECCN的描述而被归入不需要许可证的EAR99,导致大量新兴技术被外国企业获得,引起了美国对其在新兴技术领域的国际领先地位和国家安全的担忧。2020年以来,BIS不断通过修改现有的ECCN、在现有的ECCN中添加新的分段或添加新的独立ECCN来建立对新兴技术的控制。行业观察人士预测,这种控制未来可能向某些生物制药、生物材料以及新疫苗和药物扩展。[5]
同样值得注意的是,2022年9月15日美国总统拜登签署行政命令,要求美国国外投资委员会(CFIUS)加强审查对美国国家安全有影响的特定交易,其中包括了生物医药领域。[6] 该行政命令和之前的“生物制造本土化”意图趋向于一致,即优先保障美国本土供应链完整,确保美国制造的安全。支撑这一行政命令的法律正是2018年8月由美国国会通过并于2020年3月生效的《外国投资风险审查现代化法案》(FIRRMA),以及2020年美国财政部发布的《关于外国人在美国进行特定投资的规定》(Provisions Pertaining to Certain Investments in the United States by Foreign Persons)。
在FIRRMA颁布之前,美国外国投资委员会(CFIUS)仅审查可能导致美国业务被外国人控制的交易对国家安全的影响,该审查程序对跨境生物医药技术交易的缔约方约束较少。FIRRMA扩大了受CFIUS审查的交易范围,将美国企业的某些非控股外国投资也包括在内。另外,FIRRMA引入了以“关键技术”为重点的强制性申报,FIRRMA将关键技术定义为包括新兴和基础技术,这些技术的内容同2018年《出口管制改革法》(ECRA)第1758条的规定一致。以上规则直接导致跨境收购或技术交易被否决的风险大大增加。
2022年9月15日,英国生物科技公司F-star Therapeutics Inc.发布公告称,中国生物制药子公司invoX Pharma对其发起跨境收购以获得四价双特异性抗体权益的交易因未通过CFIUS 30天的例行审查,进入到为期45天的调查期,且审查时间可能继续延长。[7] 2022年9月18日,国内CXO公司凯莱英也公告宣布收购美国化学技术公司Snapdragon的交易因美国外资投资委员会(CFIUS)的反对而被终止,反对原因是Snapdragon使用美国政府资金开发其技术,而CFIUS不希望一家中国公司拥有该技术。[8] 此前CFIUS阻止中国公司对美国公司的参股投资大多涉及化工、能源、半导体等非医药领域。近期两起涉及中国医药公司的遇挫事件,释放出美国或收紧跨境生物医药技术交易的信号。
美国对生物医药技术的出口管制政策也引发了其国内各界人士的讨论。美国生物技术创新组织机构(Biotechnology Innovation Organization,BIO)提交意见,敦促美国政府全面评估生物技术出口管制对美国经济的影响以及对美国生物技术全球领导地位的潜在影响,应根据ECRA第4811(1)节中的出口管制政策声明“仅在必要的范围内”实施这些管制,以确保国家安全。在提议对特定生物技术的出口管制之前,商务部应评估对国内研究、开发或利用这些技术的美国公司投资的影响,评估每项潜在出口管制对生物技术和生命科学生态系统健康的影响,以及他们招募和留住开发部署这些技术所需的技能人才的能力。[9] 有美国学者评论道:“ 生物技术领域的国际合作是分担巨大风险和成本的一种方式,限制该领域的合作,并且无视生物医药技术的健康和福祉,以国家安全为由限制生物技术行业可能会损害美国的竞争力。”[10]
欧洲是我国创新药“出海”的第二大市场,其医药市场规模仅次于美国,同样具有发展成熟、体量庞大、增长稳定等特点。欧盟近期的政策动向显示,其或与美国同频,继续缩紧对生物医药技术出口的限制。欧盟理事会于2021年5月10日通过了《欧盟两用物项出口管制条例》(Regulation 2021/821,简称《欧盟条例》)。《欧盟条例》取代了此前欧盟两用物项出口管制主要法律文件《第428/2009号欧盟理事会规章(Regulation (EC) No. 428/2009)》,该规则在公布后的第90天生效。《欧盟条例》确定了欧盟出口管制的共同规则,设置了一系列共同的评估标准和共同的许可类型,包括欧盟通用出口许可、成员国通用出口许可、全球出口许可以及单项出口许可。在EU001~EU008八类欧盟通用许可类型中不包括对中国进行生物医药技术的出口,国内药企进行“敏感技术”的跨境交易,需向欧盟成员国当局申请并获得审批许可。
《欧盟条例》确定的管制物项清单由欧洲议会根据《瓦森纳协定》等国际共识制定并修订,其与美国EAR中的CCL分类相同,并同样采用ECCN结构对管控物项进行编码。《欧盟条例》与美国的出口管理法案相比,规定了全面控制条款(catch-all),该条款第1项规定,有关物项虽然没有列入清单,但“其全部或部分目的是或可能是在化学、生物或核武器发展的任何阶段使用”,仍需要出口核准。第2项将这一条款扩大到“全部或部分用于或可能用于军事目的”。依照该条款,出口商有义务报告他们“知道或有理由知道”可能违反两用物品条例的任何交易。受该条款影响,跨境技术交易当事人相应的负担将会增加,一旦技术交易涉及“敏感技术”,当事人就必须向欧盟成员国当局履行报告义务,以证明其不具有军事使用目的。
《欧盟条例》的通过代表欧美在对华出口管制问题上态度基本一致。2022年5月15日至16日,美国与欧盟贸易和技术理事会(Trade and Technology Council,TTC)在法国巴黎召开第二次部长级会议并发布联合声明,声明中进一步明确就美国和欧盟关键技术(包括生物医药技术)的出口进行更深入的信息交流,协调美国和欧盟的许可政策,以及与美国和欧盟以外的合作伙伴进行合作。[11] 这次的联合声明进一步释放出欧盟对医药技术出口的强监管信号。

中国医药技术出口管制的变化
医药企业在跨境技术交易过程中还会面临我国的进出口管制风险,尤其是涉及微生物、毒素等特殊技术的进出口。
我国对生物医药技术出口的管制规则分布在《出口管制法》、《技术进出口管理条例》、《生物两用品及相关设备和技术出口管制条例》等法律法规中。其中《出口管制法》是我国第一部单行立法的出口管制法规,于2020年10月通过。《出口管制法》的颁布扩展了我国传统意义上“出口”的边界,将企业经营中的技术交易、管制物项相关技术资料的传递纳入管制范围。《技术进出口管理条例》对技术出口限制做了更细致的规定,该条例明确规定了,技术进出口行为包括专利权转让、专利申请权转让、专利实施许可、技术秘密转让、技术服务和其他方式的技术转移。
作为《技术进出口管理条例》的补充,原对外经济贸易部与科学技术部编制并发布了第一版《中国禁止出口限制出口技术目录》,建立起中国技术出口的负面清单管理制度。2020年8月28日,该《目录》进行了一定的调整。在禁止出口部分,与生物医药技术相关的修改是删去了核黄素(VB2)生产工艺(编号:052702J)条目以及化学合成及半合成药物生产技术(编号:052705J)条目。修改后的禁止出口的生物医药技术包括世界珍稀、濒危保护动植物中的野生中药资源及其繁育技术;珍稀、濒危保护植物药材种质和基因资源及其繁育技术;濒危、珍稀药材代用品的配方和生产技术;菌类药材的菌种、菌株、纯化、培养、发酵和生产工艺;毒性中药的炮制工艺和产地加工技术以及常用大宗中药的炮制工艺和产地加工技术。另外,我国对其他具有保护级别的中药材物种、繁育技术及配方技术;生产菌种、毒种及其选育的生物技术药物生产技术;石斛夜光丸内重金属低于限量标准的中药配方和生产技术;组织工程医疗器械产品的制备和加工技术实施限制出口管制。
2022年1月1日起,我国开始实施最新的《两用物项和技术进出口许可证管理目录》,对于军民两用的生物医药技术也实施许可证管理,其中用于生产人及人兽共患病病原体、植物病原体、动物病原体、毒素及其亚单位、遗传物质和基因修饰生物体的相关技术在列。

国内药企如何应对
根据美国和欧盟最近的政策风向,强监管新规将很快纳入议程。而随着《出口管制法》的出台,我国重拾“对等原则”,未来也可能对特定国家实施对等的出口管制。在这一系列潜在风险的威胁下,对于国内药企来说,如何减少技术出口管制措施对技术布局的影响在未来可能成为极为紧迫的问题。在强出口监管渐呈常态化的背景下,企业要在各国出口管制交叉监管中求得发展,必须尽快全面提升自身综合性出口管制合规水平。在推进跨境License-in/out交易前,可以结合自身及外部专业人士的力量,充分了解我国以及目的的国家或地区的进出口管制政策变化,分析相关技术是否受相应的出口管制制度控制或属于“敏感技术”范畴,审查外商投资要求,研判出口管制风险。在项目磋商过程中对涉及出口管制问题影响交易目的实现的责任分担问题进行谈判,可以较大程度避免出现支付高额预付款后却难以获得许可技术的情况,降低交易风险。
注释:
[2]https://www.washingtonpost.com/technology/2022/10/27/expect-more-china-related-tech-crackdowns-us-official-says/最后访问时间:2022年10月31日。
[3]https://www.bloomberg.com/news/newsletters/2022-10-31/us-asks-europe-to-consider-export-controls-on-china最后访问时间:2022年10月31日。
[4] ECCN是瓦森纳体系下的出⼝管制分类编码,共五位,由字母和数字组成,第⼀位是十类商品控制类别序号(0-9),第二位是字母A~E(A为设备、组件、零件,B为检测设备,C为材料,D为软件,E为技术),第三位至五位是表示出口管制理由的三位数字。
[5] https://www.lexology.com/library/detail.aspx?g=ae8add10-1374-4d26-a888-eddbad57de8d最后浏览时间:2022年10月27日。
[6] https://www.kirkland.com/publications/kirkland-alert/2022/09/cfius-executive-order最后访问时间:2022年10月31日。
[7] 来源于:F-star Therapeutics公司公告。
[8] 来源于:深圳证券交易所上市公司公告。
[9]https://www.bio.org/letters-testimony-comments/bios-comment-advanced-notice-proposed-rulemaking-regarding-review最后访问时间:2022年10月31日。
[10] https://finance.yahoo.com/news/us-sanctions-china-could-extend-052143428.html最后访问时间:2022年10月31日。
[11] https://ec.europa.eu/commission/presscorner/detail/en/STATEMENT_21_4951最后访问时间:2022年10月31日。


