


近几年来,越来越多的医药企业通过跨境License-in/out模式,从境外企业引入新产品,获得在特定区域的研发、生产和销售的权利,使产品更快商业化;或将药品的海外权益对外授权以获得较高的价值变现。据医药魔方的统计数据显示,2017-2022年医药企业跨境License-in/out交易的首付款和总金额都在持续上升,其中2018-2019年License-in模式占据主流,2020-2021年License-out模式通过大单Deal实现价格反超。2021年License-in交易排名榜首的是Providence Therapeutics与云顶新耀之间的合作协议,该项目交易总额超4亿美元。其他位列top10的License-in项目交易总额也均到达亿美元级别。
2021年License-out交易排名榜首的是百济神州和诺华之间的合作协议,诺华获得百济神州TIGIT抗体的美国、加拿大、欧洲多国及日本的权益,该项目预付款3亿美元,交易总额达28.95亿美元,另有4家企业的License-out项目交易总额都突破了10亿美元。2022年上半年,License-in和License-out项目的最高交易总额也均在10亿美元以上。通过以上数据我们可以看出,医药企业跨境License-in/out交易正处于大热阶段,且交易标的额往往很高。但License-in/out协议的签订涉及诸多复杂的法律问题,如果对协议条款所潜藏的风险没有很清楚的把握就草率谈判、签订许可协议,必然会在履行许可协议的过程中触发商业风险。一旦发生争诉,往往会消耗双方大量的精力和财力,而且诉讼还可能会久判不决,诉讼结果也难以预期。
本文结合多年服务经验,与读者分享跨境License-in/out协议的审查要点。一份完整的License-in/out技术许可协议主要包括定义(Definitions)、授权(License Grants)、许可费用(Payment)、知识产权(Intellectual Property)、产品制造与商业化(Manufacturing and Commercialization of Product)、陈述与保证(Representations and Warranties)、终止条款(Term and Termination)、争议解决(Dispute Resolution)等部分。本文将重点围绕这些条款进行展开。

定义条款(Definitions)
1.拟许可产品及技术
对拟许可的专利(Licensed Patent)、专有技术(Licensed Know-how/Licensed Technology)、产品(Licensed Product)应做范围明确、完整的界定。可通过附表的形式列出拟许可专利的具体专利号,对不能形成专利文件的专有知识诀窍用“专有技术”的定义和描述来实现最大程度的涵盖。
2.领域(Field)
对授权领域的定义需要考虑是否明确适用对象(human/ non-human)、诊疗方式(therapeutic/ diagnosis/ prevention),对有多项治疗靶点或适应症的药品是否限制诊疗领域(brain tumors/ stomach ulcers),若许可人意图保留其他领域的商业化权利,可以采用“but no other use”的表述。[1]
3.地域(Territory)
对地域的定义通常需要明确一项许可是全球性还是区域性,全球性的许可一般表述较为简单(entire world),区域性的许可应当注意说明具体的国家或范围,对可能造成模糊、不统一的表述如“North America”“European Union”进行进一步的定义,或通过附表的形式对授权国家及地区予以列举。当被许可方是中国企业时,还应当特别写明授权地域是否包含我国的香港、澳门及台湾地区,避免双方因对授权地域理解不一引发纠纷。

授权条款(License Grants)
1.授权类型
授权类型包括非排他许可(Non-Exclusive License)、排他许可(Sole License)、独占许可(Exclusive License)三种。对Non-Exclusive License鲜少有理解偏差,需要关注的是Sole License、Exclusive License分别对应中国法语境下的排他许可和独占许可。在Sole License中,许可人不能将被授权的权益再授予第三人,但可以自己使用;而在Exclusive License中排除了许可人自己的使用。
2.分许可(Sub-License)
许可人是否保留分许可的权利,被许可人需要履行怎样的分许可程序也是双方谈判及合同审查中需要重点关注的条文。有权分许可的对象如何确定,仅限于被许可人的关联机构还是可以扩展到外部第三人?被许可人进行分许可应当如何履行通知义务?是否需要获得许可人的同意?许可人是否对被许可人分许可进行其他的限制?分许可的收入是否纳入交易费用结构?这些问题都应当在交易协议中作出具体的约定。
3.许可冲突(Limitations on Other Licenses)
在非排他性许可的情况下,被许可一方尤其需要注意许可冲突条款的拟定,以避免许可人有在先的冲突许可带来潜在的竞争。被许可方可要求许可人就不存在在先的冲突许可及在协议有效期内不进行冲突许可作出陈述保证。
许可费用条款(Payment)
由于药品从研发到上市的过程较为漫长,考虑到不同阶段新药的估值水平和企业的资金实力,目前较为合理的交易费用是分阶段付款:预付款(Upfront Payment)+ 里程碑付款(Milestone Payment)+ 许可使用费(Royalty Payment)。这种交易安排一方面可以减少潜在买方短期的资金压力,另一方面许可方可以在后续产品上市后获得较高比例的销售收入分成。相比一次性付清的许可费用,这种交易安排大大提高了项目转让的成功率。
1.预付款(Upfront Payment)
预付款是指被许可方在许可期开始时或接近许可期开始时向许可方一次性支付的费用,预付款的金额受许可方就许可标的已投入的成本、许可标的市场价值和潜力、引进方的资金实力等诸多因素影响。一方面,许可人希望尽可能提高预付款的金额以收回投入成本,并对冲不确定的未来收益;另一方面,被许可人更青睐降低预付款的金额,以保证产品商业化拥有足够的现金流,抓住上市窗口。预付款的确定依赖于交易双方对授权产品未来收益的预测,双方可以通过交易谈判调整预付款和销售分成的比例结构。许可方一般会在协议中约定预付款不可返还、不可抵销(non-refundable and non-creditable),在签订协议前应当对这部分条款予以充分的注意,避免当被许可产品的开发效果不如意或被许可方中途放弃开发的情况发生后,双方就相关事项发生争议。
2.里程碑付款(Milestone Payment)
里程碑付款是指交易方在某项“里程碑事件”完成后才支付相应的交易款项。里程碑事件可基于商业化成就,也可基于研发进展。里程碑事件的触发是交易双方最易发生争议的地方,里程碑事件的设计应当尽量明确界定为在产品研发计划或商业化战略中各方合理预期应达成的某些具体的客观事件,避免使用主观描述。
典型的里程碑事件有:
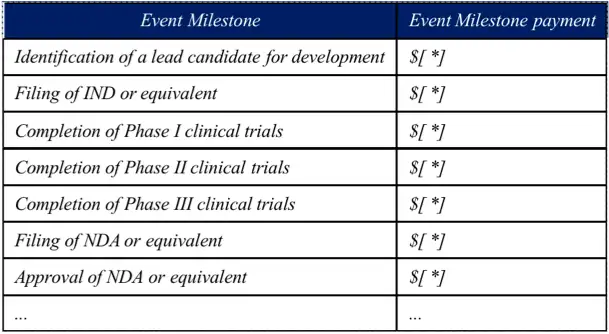
同时协议中对“完成”里程碑事件的约定也是双方争议高发的条款。尤其应当避免采用里程碑事件的成功完成(successful completion)或令人满意的完成(satisfied completion)等类似表述,双方可能对“successful”“satisfied”的程度理解不一。被许可人倾向于认为表现出较大开发潜力的开发进展才触发付款条件,但许可人显然更喜欢降低标准,因为即使被许可人对临床试验的结果不满意,许可人也会获得里程碑付款。为了避免该类分歧,可以在许可协议中规定,下一个阶段的开始被视为前一阶段圆满完成的证据:“Commencement of Phase II clinical trials means that Phase I clinical trials have been successfully completed.”[2]
3.许可使用费(Royalty Payment)
许可使用费的计算总体上是基于“净销售额”(Net Sales)的一定费率比例。在双方谈判确定相应比例的情况下,净销售额的统计将对许可使用费产生较大的影响。净销售额在会计学意义上指总销售额减去退货、补贴和折扣的结果,不同的会计方法将会导致净销售额有较大额的差别,双方在交易谈判中应当对净销售额的含义进行明确界定。可以予以扣减的款项包括:退货、退单、降价、销售佣金、销售税、消费税、关税以及运费等支出,协议中应尽可能详细地列明具体的扣减款项。
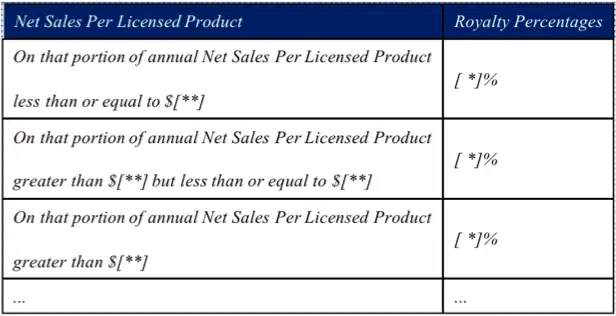
另外,交易协议中对许可费用扣减机制的约定也至关重要。在较长的药品研发期,可能出现多项事由导致被许可方预期收益减损。比如:专利受到无效挑战或在相应区域内到期、市场上出现仿制药的销售、竞争产品已经实现商业化等。被许可方有必要在协议中写明许可费用的扣减机制。另外,作为许可人一方,应当注意约定明确约定扣减底线(Reduction Floor):“In no event may the royalty be reduced by more than [*].”,避免丧失全部的许可费权益。
4.定期付款(Periodic Payments)
除上文所述的预付款、里程碑付款、许可使用费外,当事人还可以约定一定数额的定期付款。该部分款项通常在开始收取许可费前(产品进入商业销售状态)停止计费。被许可方如果不打算开发利用被许可技术,则它可能不愿意支付无期限的定期费用。从许可方的角度来看,在交易费用中引入定期付款,可以用于激励被许可人积极开发、运用被许可技术,而在产品开发无进展的情形下也可获得一定的经济利益。
产品制造与商业化(Manufacturing and Commercialization of Product)
在此条款下,为了保证产品制造与商业化进程推进,交易双方一般会在协议中对被许可方的勤勉义务作出约定。目前协议中通常的写法是:被许可方应尽到商业上的合理努力(Commercially Reasonable Efforts,简称“CRE”)。CRE是大型商业交易中经常用到的一个表述,一般认为,CRE的努力程度要低于最大努力(best efforts),但具体到交易行为中该如何判断一直没有非常明确判断标准。为更加有效地约束被许可方,可以在协议中就具体的研发和销售目标作出相关约定,同时还可以约定被许可方的定期报告义务。

知识产权条款(Intellectual Property)
在知识产权条款下,应关注对知识产权维护和维权的约定,明确各方责任。如哪方应当承担知识产权的日常维护责任?相关费用如何承担?被许可技术遭遇侵权,哪方应当主动发起维权?维权所得收益如何在当事人之间进行分配?在此条款下,还需关注技术改进(Technology Improvement)的相关表述。值得注意的是,若许可方限制被许可人技术改进的权利可能触发反垄断审查,具体是否可以限制一方技术改进的权利,应考虑协议约定适用法律对此是否有强制性规定。在中美贸易谈判的大背景下,我国的《技术进出口条例》几经修改,最新修订的《技术进出口条例》已经删除了对技术许可合同的限制性的强制规定。删除的条款规定技术进口合同中不得限制受让人改进转让方提供的技术或者限制受让人使用改进技术。
但实际上,这些条款的内容几乎和《技术许可合同司法解释》第十条的规定是一致的。《技术许可合同司法解释》第十条[3]规定了限制一方当事人技术改进属于“非法垄断技术”,应当无效。因为两者都属于强制性条款,司法解释的条款仍可以作为谈判中的重要砝码。但在具体实践中,如果交易双方约定适用外国法律和境外仲裁,境外仲裁机构可能较难援引司法解释的强制性规定来判定相关条款无效。交易双方更应该通过谈判谋求相关利益,并在合同条款起草时慎之又慎,尽量减少争议发生后相关利益的损失。《技术进出口条例》的修改为当事人提供了更大的协商空间,这也对相关企业的谈判能力和合同起草水平提出了更高的要求。在被许可方有充分的潜力对技术进行改进的情形下,约定技术改进的知识产权归属及相关权利归改进方所有,同时为许可人设置非排他的、免费(non-exclusive,royalty-free)的权利回授条款(grant-back)似乎是双方更容易接受的谈判结果。

陈述与保证(Representations and Warranties)
在此条款下,首要关注许可方应保证其是专利技术的合法所有者,并有权进行技术转让,这种转让在协议规定的地域内没有侵犯任何第三方的权利。上述对专利权属的保证条款可以较大程度减少第三方侵权发生的风险。除此之外,被许可方在谈判中可以考虑基于双方的合作关系、同类合同的惯例以及风险承担的分配等理由,说服许可方接受对第三方侵权承担一定责任。例如,可以将第三方侵权发生约定为许可费扣减事由以及约定许可方对特定第三方侵权承担部分赔偿责任等。
终止条款(Termination)
License-in/out交易一般囊括了医药研发、生产和商业化的整个阶段,履行时间长,通常伴随专利权的整个有效期。且专利最终还要进入公有领域,在这么长的时间内很难保证双方当事人时时处处积极履行好自己的权利义务。同时,License-in/out交易标的往往数额巨大,交易双方需要谨慎地酌定终止事项及拟定终止条款。在License-in/out交易中,往往会规定被许可方享有自由解除合同的权利(terminate for convenience)。而许可方也可以在协议中约定解除合同的事由,如被许可方未能按时履行付款义务或未能达到预期的研发和销售目标等。
被许可方可以在多种情况下自由解除合同,以终止项目开发:如药品后续的研发进展未达预期、预期商业化回报估算偏差或许可方迫于后续资金压力或调整研发赛道等等。一个License in/out项目的终止,并不意味着相关技术或药品被宣判失败。在“非研发失败”的情况下,被许可方解除合同将可能使得技术权益再次回到许可方手上,许可方仍然可以再次利用开发。
在License-in/out项目推进过程中,被许可方就药品前期研究付出了较大的投入,可能形成了潜在药品开发过程中产生的信息和数据的集合,如毒理学研究和临床试验结果。药品研发都要经过“不断试错”的过程,这部分的研究结果本身就具有较高的价值。则在许可协议提前终止的情况下,如何对药品开发文件进行处理?研发的前期投入如何进行分配补偿?技术后期权益归属于何方?这些问题都是交易双方在谈判终止条款时应当注意的问题。
2021年8月,信立泰发布公告终止与美国VIRACTA签订的关于抗肿瘤药“nanatinostat”的《独家许可使用协议》,VIRACTA将向信立泰支付400万美元(约2600万元人民币)用于补偿其前期研究及合作贡献,信立泰则将返还或销毁nanatinostat有关资料,所产生的费用由信立泰承担。[4]在这个案例中,信立泰公司自2018年开始该项License-in项目,至协议终止时,“nanatinostat”项目有关技术转移尚未完成,未取得实质性进展,亦未支付许可使用费用。
但交易双方应当考虑的是,随着药品研发进程的推进,有关研发文件将不断增加,协议解除后有关补偿问题也会变得愈发复杂。具体补偿条款如何约定,双方可以基于对项目预期收入的估计进行谈判,同时补偿金额也要根据项目研发进程、未来商业化前景等做到梯度设计。在实践中可以考虑约定:被许可方终止协议后,许可方将产品商业化,补偿给被许可人一定比例的销售分成;若许可方将技术许可给第三人继续进行商业化开发,则补偿被许可人一定比例的许可使用费、里程碑费用,或就被许可人前期研发投入进行一次性的补偿。
另外,根据不同的项目开发进程合理商定不同的补偿比例。例如,如果被许可人提前终止协议发生在临床前试验期间,但在提交IND之前,被许可人有权从许可人处获得[*]%的销售分成,如果许可人许可给第三方,则补偿额为第三方支付给许可人的所有金额的[*]%,以及报销一定比例的被许可人临床前工作产生的自付费用。如果协议终止发生在产品获得监管部门批准后,补偿金的比例则予以调整。
争议解决(Dispute Resolution)
1.适用法律
适用法律依赖于交易双方的谈判,在对适用法律的选择上,若不能选择适用中国法,从中立角度可以考虑选择不在一方所在地的新加坡、英格兰与威尔士、香港等国家或地区法律或者其他企业较为熟悉的国家或地区的法律。
2.争议解决方式
仲裁对交易双方来说是私密性、友好性都更优的争议解决方式,通过仲裁程序当事人可以引入对医药领域科学技术问题有深入理解的行业专家。对于中方企业来说,通常情况下建议尽量选择中国作为仲裁地,在无法选择中国作为仲裁地的时候,可以选择新加坡、香港等第三方地区,以更方便选择具有中文文化背景的仲裁员。
结语
License-in项目已经成为药企补充自身产品管线的有效手段,License-out项目也成为国内药企创新出海的有力证明。但项目成就同时意味着背后有长达几年的研发期和高达亿美元以上的交易总额,在协议签订前的谈判及合同起草审查阶段应当关注到跨境许可涉及的诸多复杂的法律问题,并及时调整谈判策略及协议内容,以争取最大化的商业利益。
注释:
[1]https://fslaw-asia.com/four-key-terms-in-a-licensing-agreement/ 最后访问时间:2022年9月7日。
[2]https://www.morse.law/news/biotech-patent-licensing/ 最后访问时间:2022年9月7日。[3]《最高人民法院关于审理技术合同纠纷案件适用法律若干问题的解释》第十条规定:下列情形,属于合同法第三百二十九条所称的“非法垄断技术、妨碍技术进步”:
(一)限制当事人一方在合同标的技术基础上进行新的研究开发或者限制其使用所改进的技术,或者双方交换改进技术的条件不对等,包括要求一方将其自行改进的技术无偿提供给对方、非互惠性转让给对方、无偿独占或者共享该改进技术的知识产权;
(二)限制当事人一方从其他来源获得与技术提供方类似技术或者与其竞争的技术;
(三)阻碍当事人一方根据市场需求,按照合理方式充分实施合同标的技术,包括明显不合理地限制技术接受方实施合同标的技术生产产品或者提供服务的数量、品种、价格、销售渠道和出口市场;
(四)要求技术接受方接受并非实施技术必不可少的附带条件,包括购买非必需的技术、原材料、产品、设备、服务以及接收非必需的人员等;
(五)不合理地限制技术接受方购买原材料、零部件、产品或者设备等的渠道或者来源;
(六)禁止技术接受方对合同标的技术知识产权的有效性提出异议或者对提出异议附加条件。[4]信息来源:深圳证券交易所上市公司公告。


